【摘要】集中资源攻克衰老已成共识。AI与资本正驱动抗衰科学从分散探索转向系统工程,重塑健康寿命的未来。
引言
全球人口结构正在经历深刻转变。老龄化与慢性病负担的加剧,促使我们将目光从单纯延长生命(Lifespan)转向提升健康生命(Healthspan)。在这一背景下,一个宏大的构想开始浮现,即发起一场“衰老研究的曼哈顿计划”。这个提法并非空穴来风。它主张借鉴历史经验,将曾经用于原子能、登月或人类基因组测序的集中式、工程化攻坚模式,应用于抗衰老这一复杂命题。
当前,科技资本、顶级研究机构与人工智能技术正以前所未有的力度汇聚于此。抗衰老科学正悄然经历一场范式革命,从零散的实验室探索,逐步升级为一门数据驱动的、目标明确的系统工程。本文将深入剖析这一计划的内涵、核心驱动力、技术实现路径,并客观评估其面临的体系性障碍与未来发展路线。
一、概念与目标:系统工程的黎明
%20拷贝.jpg)
1.1 “曼哈顿计划”的现代内涵
所谓“衰老研究的曼哈顿计划”,其核心并非简单复刻历史,而是借鉴其组织哲学。它代表着一种高度协同的、目标导向的科研组织模式。具体内涵包括:
跨学科人才集结。它要求生物学家、数据科学家、临床医生、伦理学家和工程师等不同领域的专家紧密协作。
资源集中投入。它需要国家级、乃至全球级的资金、算力与数据资源进行战略性配置,支持高风险、长周期的基础研究。
工程化路径管理。它强调将复杂的科学问题分解为可执行、可验证的工程模块,并设定清晰的里程碑与交付目标。
这种模式的本质,是将抗衰老研究从“科学家个人兴趣驱动的探索”转变为“社会共同目标驱动的攻坚”。
1.2 核心目标:延长健康寿命(Healthspan)
此计划的最终目标极为明确,即最大化人类的健康寿命。这与单纯延长寿命存在本质区别。
将衰老本身视为一种可干预的生物学过程,而非不可避免的自然规律,是该计划的理论基石。通过干预衰老的底层机制,有望系统性地延缓多种年龄相关疾病(如心血管疾病、神经退行性疾病、癌症)的发生,实现“健康老去”。
二、驱动力集结:跨界联盟的形成
一场“曼哈atan计划”级别的行动,离不开强大驱动力的汇聚。当前,一个由科技巨头、风险资本和思想领袖构成的跨界联盟已初步形成。
2.1 科技企业与研究机构
科技企业,特别是AI领域的领导者,正成为这场变革的策源地。
OpenAI生态与Sam Altman。Sam Altman个人对Retro Biosciences的巨额投资(种子轮1.8亿美元)及其后续的资金承诺,是资本与技术领袖深度介入的标志性事件。这背后是其对AI与生物技术结合能够解决根本性问题的坚定信念。
Google DeepMind与AlphaFold。AlphaFold项目通过AI精准预测了超过2亿种蛋白质的结构,从根本上改变了结构生物学和药物研发的范式。这一基础科学工具的突破,为寻找抗衰老靶点提供了前所未有的效率。它将过去需要数年实验验证的蛋白质结构解析工作,缩短到了数天甚至数小时。
这些机构的入局,不仅带来了资金,更重要的是带来了海量算力、顶级AI人才和工程化的思维方式。
2.2 风险资本与专项基金
长寿科技领域正吸引着越来越“耐心”的资本。
Retro Biosciences。其目标明确,即通过细胞重编程等技术,在10年内将人类健康寿命延长10年。这种目标驱动的模式吸引了大量长期资本。
age1。由Laura Deming等人创立的这家公司,专注于投资早期抗衰老技术。它不仅提供资金,还构建了一个连接科学家、企业家和投资者的生态系统,加速了从实验室到市场的转化。
这些专项基金的出现,解决了传统VC对长周期、高风险生物科技项目望而却步的痛点,为前沿探索提供了关键的早期支持。
2.3 思想领袖与社会共识
在各类会议、演讲和公共讨论中,关于长寿和AI的议题热度持续攀升。以Laura Carstensen等学者为代表的思想领袖,从心理学、社会学角度探讨长寿的积极意义,为技术发展提供了人文关怀的视角。这种跨界讨论正在逐步构建社会共识,即投资长寿研究不仅是一项技术挑战,更是一项关乎人类福祉的社会事业。
三、AI的核心引擎角色
%20拷贝.jpg)
如果说资本和人才是燃料,那么AI就是这场计划的核心引擎。AI技术在抗衰老研究的全链条中都扮演着不可或-缺的加速器角色。
3.1 基础科学:从序列到结构与功能
在生命科学的基础层面,AI正在破译生命的底层密码。
蛋白质结构预测。AlphaFold是其中的典范。蛋白质是生命活动的主要执行者,其三维结构决定了其功能。准确预测蛋白质结构,是理解疾病机理和设计靶向药物的第一步。
基因组学与靶点发现。AI模型能够分析海量的基因组、转录组和蛋白质组数据(多组学数据),识别与衰老相关的关键基因通路和潜在药物靶点。传统方法在这种数据维度下面临“维度灾难”,而AI则游刃有余。
3.2 药物发现与分子设计
AI正在彻底颠覆传统的药物研发流程。
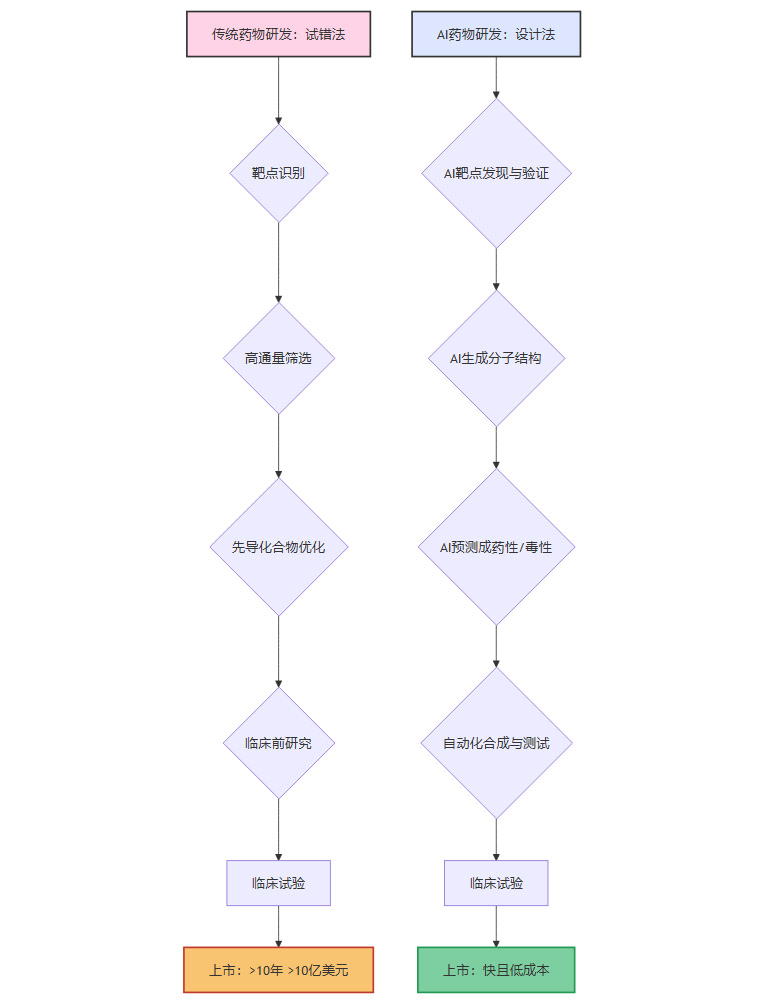
虚拟筛选。AI模型可以在数小时内从数十亿个分子库中筛选出可能对特定靶点有效的候选化合物,效率远超物理筛选。
分子生成。更进一步,生成式AI模型(如GNN、Transformer)可以从零开始设计具有特定化学性质和生物活性的全新分子结构,即“AI制药”。
ADMET预测。AI能够预测候选药物的吸收(Absorption)、分布(Distribution)、代谢(Metabolism)、排泄(Excretion)和毒性(Toxicity),在研发早期就剔除失败风险高的分子,大幅降低了后期临床试验的失败率。
3.3 临床应用:精准与预测
在临床端,AI的应用同样广泛。
生物年龄时钟(Aging Clocks)。通过分析血液、DNA甲基化等数据,AI可以构建比生理年龄更精确的“生物年龄”模型。这为评估抗衰老干预措施的有效性提供了可量化的生物标志物。
风险分层与早期预警。AI模型能够整合电子病历、医学影像、可穿戴设备数据,对个体未来的疾病风险进行精准预测,实现从“被动治疗”到“主动预防”的转变。
个性化干预方案。基于个体的基因组和生活方式数据,AI可以推荐最优的营养、运动乃至药物干预方案,实现真正的个性化健康管理。
3.4 核心依赖:数据、算力与算法的铁三角
AI的强大能力并非凭空而来。它建立在一个稳固的“铁三角”之上。
高质量数据。这是AI模型的“燃料”。特别是纵向队列数据(即对同一个人群进行长达数年甚至数十年的跟踪随访),对于衰老研究至关重要。数据的标准化、清洁度和完整性直接决定了模型性能的天花板。
大规模算力。训练先进的生命科学AI模型(如AlphaFold)需要巨大的计算资源。GPU集群、TPU等专用硬件是开展大规模研究的必备基础设施。
先进算法。从经典的机器学习到深度学习,再到最新的图神经网络和生成模型,算法的持续创新是提升模型精度和解释性的关键。
这三者缺一不可。任何一个环节的短板,都会限制整个“曼哈顿计划”的推进速度。
四、代表性进展与前沿案例
尽管宏伟蓝图仍在铺开,但一些标志性的进展已经出现,验证了这一路径的可行性。
4.1 跨物种研究与转化
犬类长寿治疗评估。Loyal公司正在对约1300只狗进行长寿治疗评估。狗的衰老速度比人类快,且与人类生活在相似环境中,使其成为研究抗衰老干预的理想模型。这类研究能够以更短的时间周期,为人类疗法提供宝贵的安全性和有效性数据。
异种移植探索。一名男子成功接受猪肾移植并存活一段时间,是异种移植领域的阶段性突破。尽管挑战重重,但它为解决器官短缺问题提供了一种潜在方案,直接关系到老年群体的生命质量。
4.2 基因与细胞疗法
个体基因治疗。听力受损幼儿Opal Sandy通过基因治疗恢复听力的案例,展示了基因编辑技术在修复与衰老相关的感官功能缺陷方面的巨大潜力。衰老过程中的许多功能衰退,本质上与特定基因的表达异常有关。
细胞重编程。Retro Biosciences等公司正在探索通过重编程技术“逆转”细胞年龄。虽然距离临床应用尚远,但其在细胞层面展现出的“返老还童”潜力,使其成为长寿研究中最受关注的前沿方向之一。
4.3 “长寿药丸”的前景与审慎
业界存在一种乐观预测,即“几年内可能出现某种形态的长寿药物”。这类药物可能靶向mTOR、AMPK等已知的衰老信号通路。
然而,对此必须保持审慎。
监管路径。目前,美国FDA等监管机构并不将“衰老”本身视为一种疾病。这意味着任何抗衰老药物都需要以预防或治疗某种特定年龄相关疾病(如骨质疏松)的名义进行审批,这增加了临床试验设计的复杂性。
临床证据。从动物实验的成功到在人类身上证明安全有效,需要大规模、长周期的随机对照试验。任何声称的“长寿药丸”都必须经过这一严谨的循证医学检验。
五、体系性障碍与现实挑战
%20拷贝.jpg) 通往长寿的“曼哈顿计划”并非坦途。它面临着深刻的体系性障碍。
通往长寿的“曼哈顿计划”并非坦途。它面临着深刻的体系性障碍。
5.1 数据层面的挑战
5.2 临床与监管的障碍
高昂的协同成本。跨机构、跨国界的大规模临床研究,面临巨大的沟通、管理和执行成本。
可重复性危机。生物医学研究本身就存在一定的可重复性问题。AI模型的“黑箱”特性可能加剧这一问题,需要建立严格的外部验证和可解释性AI(XAI)机制。
滞后的审批体系。当前的药品和疗法审批体系是为“治疗已病”设计的。对于旨在“预防未病”的抗衰老干预,缺乏成熟的评估标准和审批路径。
支付体系的错配。医保和商业保险通常按次付费,为已发生的疾病买单。如何为一项可能在十年后才显现效果的预防性干预付费,是商业模式上的巨大挑战。
5.3 伦理与公平性的拷问
伦理边界。异种移植、基因编辑、细胞重编程等技术都触及深刻的生命伦理问题。动物实验的福利、数据隐私与所有权(数据主权)等都需要社会层面的广泛讨论和共识。
公平可及性。初期,先进的抗衰老疗法必然价格高昂。如何防止其成为少数富人的特权,加剧社会不平等,是一个必须前置考虑的治理难题。若不能实现普惠,其社会价值将大打折扣。
六、关键基础设施建设
要克服上述障碍,推动“曼哈顿计划”从概念走向现实,必须系统性地建设一系列关键基础设施。这如同为登月计划建造发射塔和测控网络,是成功的先决条件。
6.1 数据与算力基础设施
面向衰老的多组学与纵向队列数据库。
目标。建立国家级、甚至全球联盟级的生物银行(Biobank)和纵向队列研究数据库。
内容。应包含参与者长期的基因组、转录组、蛋白质组、代谢组、微生物组等多组学数据,并与电子病历、生活方式问卷、可穿戴设备数据进行关联。
范例。英国的UK Biobank、美国的All of Us研究计划是很好的参照,但需要更侧重于衰老标志物的动态追踪。
可信算力与安全沙盒。
目标。为研究人员提供一个既能访问海量敏感数据,又能确保数据不出域、隐私不泄露的安全计算环境。
技术。利用联邦学习(Federated Learning)技术,模型可以在本地数据上进行训练,只交换模型参数而非原始数据。安全沙盒(Secure Sandbox)则提供一个受控的虚拟环境,对数据访问和计算操作进行严格审计。
6.2 评测与监管基础设施
医疗AI评测标准与基准(Benchmark)。
目标。建立一套公认的、标准化的评测体系,用于评估抗衰老相关AI模型的性能、稳健性、公平性和可解释性。
内容。应包含标准化的数据集、评测指标(Metrics)和排行榜(Leaderboard),类似于ImageNet在计算机视觉领域的角色。这有助于避免“自说自话”,促进技术的良性竞争。
适应性监管路径与沙盒。
目标。为颠覆性的抗衰老疗法和AI诊断工具设立“监管沙盒”(Regulatory Sandbox)。
机制。允许创新产品在有限的范围、受控的风险下进行真实世界测试,监管机构可以与开发者同步学习、迭代监管规则。这比传统的瀑布式审批模式更具灵活性。
6.3 模型与评估框架
跨物种与跨阶段转化模型。
目标。开发能够更准确地将从模式生物(如果蝇、小鼠、犬)获得的研究成果,外推到人类身上的计算模型。
方法。利用比较基因组学和系统生物学,建立物种间的生物通路对应关系,提高临床前研究的预测价值。
真实世界证据(RWE)与结局评估框架。
目标。建立一套框架,用于收集和分析来自真实医疗环境的数据(而非严格受控的临床试验),以评估抗衰老干预在长期、大规模人群中的真实效果和安全性。
价值。RWE是连接临床试验与实际临床实践的桥梁,对于评估预防性干预的长期价值至关重要。
七、伦理与社会治理框架
%20拷贝.jpg)
技术的发展必须与社会伦理和治理框架同步演进,否则可能引发不可控的风险。
7.1 防止过度承诺与科学炒作
透明度与可追溯性。要求所有研究,特别是临床试验,进行预注册,并公开其研究方案、数据和结果(无论好坏)。这有助于防止选择性发表阳性结果,提高科学的可信度。
负责任的沟通。科学家、媒体和企业在向公众传播研究进展时,应避免使用“神药”、“永生”等夸大性词汇,清晰地沟通技术的不确定性和潜在风险。
7.2 核心伦理议题的治理
动物福利。在进行大规模动物实验(如犬类研究)时,必须遵守严格的动物福利伦理准则,确保实验的必要性和人道性。
数据主权与隐私。必须明确个人对其健康数据的所有权和控制权。数据的使用应遵循“知情同意”原则,并为个人提供撤回授权的权利。
公平可及性。在研发早期就应引入卫生经济学家和政策制定者,探讨如何通过公共采购、分层定价、医保覆盖等机制,确保最终成果能够惠及最广泛的人群,而非仅仅是少数精英。
八、成功衡量指标:量化健康未来
一个“曼哈顿计划”需要清晰、可量化的成功指标。对于衰老研究,这些指标应超越传统的临床终点。
九、路线图建议:分阶段推进
%20拷贝.jpg)
一个务实的计划需要分阶段的路线图。
9.1 近期(3–5年):奠定基础
目标。建成标准化的数据基础设施和AI评测试点。
行动。
启动至少一个国家级万人规模的深度多组学纵向队列研究。
建立首批医疗AI监管沙盒,针对低风险的诊断类AI产品进行试点。
资助若干个高潜力的示范性临床项目,例如针对特定衰老通路的小分子药物I/II期临床试验。
9.2 中期(5–10年):形成闭环
目标。在高负担疾病领域形成“预防-干预-随访”的闭环,并与支付体系初步联动。
行动。
在心血管、代谢、神经退行性疾病等领域,将基于AI的风险预测模型整合进临床决策支持系统。
推动至少1-2种被证明有效的抗衰老干预(药物或生活方式)纳入部分地区的预防性医保覆盖范围。
建立成熟的真实世界证据收集与评估体系,持续监控干预措施的长期效果。
结论
长寿研究正站在一个历史性的十字路口。AI与资本的深度融合,为其从零散探索跃升为“新时代的曼哈顿计划”提供了前所未有的机遇。这不再是科幻小说,而是一个正在发生的、由代码和资本共同驱动的工程现实。
然而,这条道路充满挑战。数据孤岛、监管滞后、伦理争议和公平性问题,是横亘在我们面前的座座大山。要成功实施这一计划,需要的不仅是技术上的突破,更需要我们在数据共享、监管创新和社会治理上展现出同等的智慧和勇气。
我们必须管理好社会预期。研究进展虽快,但实现全民可及的临床转化仍需漫长的循证积累。在这个过程中,坚持稳健的科学验证、保持公开透明的沟通、审慎应对伦理风险,远比追求一蹴而就的“神药式突破”更为关键。最终,这场计划的成功与否,将由一个最朴素的标准来衡量,那就是它能否为更多人带来更长久、更健康的岁月。
📢💻 【省心锐评】
抗衰老正从生物学问题,演变为一个数据驱动的系统工程。AI是核心引擎,但数据、监管和伦理是决定其能否安全抵达终点的三大路基。

.png)
%20%E6%8B%B7%E8%B4%9D.jpg)

评论